בוועידת החיסונים והבריאות קראו מומחים "על כולם לשים לב לחיסוני mRNA, המספקים לבני אדם חשיבה בלתי מוגבלת".אז מהו בעצם חיסון mRNA?איך זה התגלה ומה ערך היישום שלו?האם זה יכול להתנגד ל-COVID-19 המשתולל ברחבי העולם?האם המדינה שלי פיתחה בהצלחה חיסון mRNA?היום, בואו נלמד על העבר וההווה של חיסוני mRNA.
01
מהו mRNA בחיסוני mRNA?
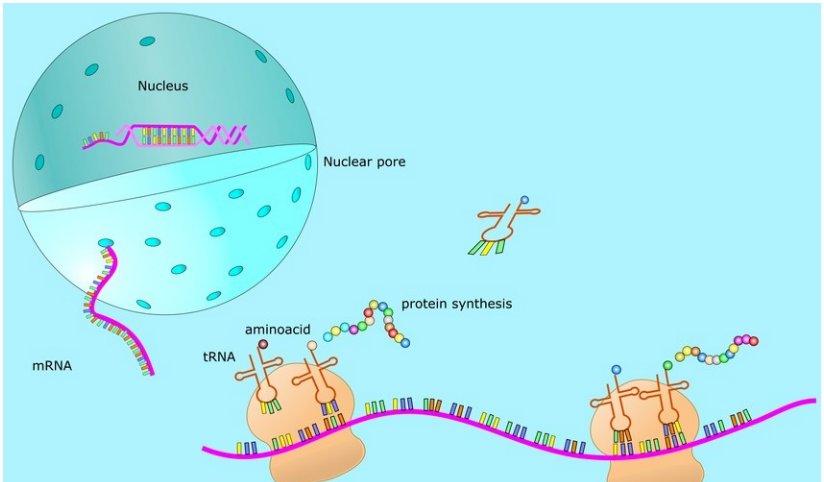
mRNA (Messenger RNA), כלומר, RNA שליח, הוא סוג של RNA חד-גדילי שמתעתק מגדיל DNA כתבנית ונושא מידע גנטי שיכול להנחות את סינתזת החלבון.במונחים של הדיוט, mRNA משכפל את המידע הגנטי של גדיל אחד של DNA דו-גדילי בגרעין, ולאחר מכן עוזב את הגרעין כדי לייצר חלבונים בציטופלזמה.בציטופלזמה, הריבוזומים נעים לאורך ה-mRNA, קוראים את רצף הבסיס שלו ומתרגמים אותו לחומצת האמינו המתאימה לו, ובסופו של דבר יוצרים חלבון (איור 1).
איור 1 תהליך עבודה mRNA
02
מהו חיסון mRNA ומה מייחד אותו?
חיסוני mRNA מכניסים לגוף אנטיגנים ספציפיים למחלה ומשתמשים במנגנון סינתזת החלבון של התא המארח כדי ליצור אנטיגנים, ובכך לעורר תגובה חיסונית.בדרך כלל, ניתן לבנות רצפי mRNA של אנטיגנים ספציפיים על פי מחלות שונות, לארוז ולהעביר לתאים על ידי חלקיקי ננו-נשאי שומנים חדשים, ולאחר מכן משתמשים ברצפי ה-mRNA של ריבוזומים אנושיים כדי לתרגם את רצפי ה-mRNA לייצור חלבוני אנטיגן מחלה, אשר מזוהים על ידי המערכת האוטואימונית לאחר הפרשה כדי ליצור תפקיד חיסוני כדי להשיג את התגובה החיסונית (Figur).
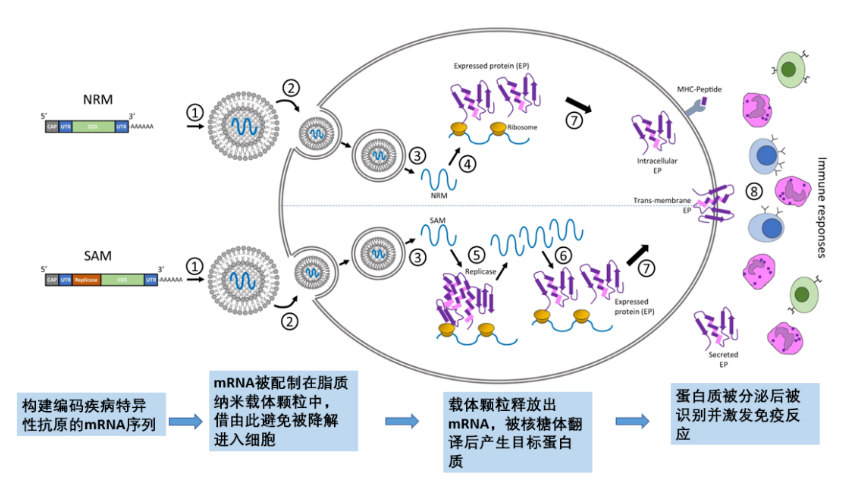 איור 2. השפעה In vivo של חיסון mRNA
איור 2. השפעה In vivo של חיסון mRNA
אז מה ייחודי בסוג זה של חיסון mRNA בהשוואה לחיסונים מסורתיים?חיסוני mRNA הם חיסוני הדור השלישי החדשניים ביותר, ויש צורך במחקר נוסף כדי לשפר את יציבותם, לווסת את האימונוגניות שלהם ולפתח טכנולוגיות מסירה חדשות.
הדור הראשון של החיסונים המסורתיים כולל בעיקר חיסונים מומתים וחיסונים חיים מוחלשים, שהם הנפוצים ביותר.חיסונים מומתים מתייחסים לגידול תחילה של וירוסים או חיידקים, ולאחר מכן השבתתם באמצעות חום או כימיקלים (בדרך כלל פורמלין);חיסונים חיים מוחלשים מתייחסים לפתוגנים שעוברים מוטציות ומחלישות את הרעילות שלהם לאחר טיפולים שונים.אך עדיין שומר על האימונוגניות שלו.חיסון זה בגוף לא יגרום להופעת מחלה, אך הפתוגן יכול לגדול ולהתרבות בגוף, לעורר את התגובה החיסונית של הגוף ולמלא תפקיד בהשגת הגנה ארוכת טווח או לכל החיים.
הדור השני של חיסונים חדשים כולל חיסונים תת-יחידות וחיסוני חלבון רקומביננטי.חיסון תת-יחידות הוא חיסון תת-יחידות חיסון העשוי ממרכיבי האימונוגן המגנים העיקריים של חיידקים פתוגניים, כלומר באמצעות פירוק כימי או פרוטאוליזה מבוקרת, מבנה החלבון המיוחד של חיידקים ווירוסים מופק ומסונן החוצה.חיסונים עשויים משברים פעילים מבחינה אימונולוגית;חיסוני חלבון רקומביננטי הם חלבונים רקומביננטיים של אנטיגן המיוצרים במערכות ביטוי שונות של תאים.
הדור השלישי של חיסונים חדשניים כולל חיסוני DNA וחיסוני mRNA.זה להחדיר ישירות את קטע הגן הנגיפי (DNA או RNA) המקודד לחלבון אנטיגני מסוים לתאים הסומטיים של בעלי החיים (הזרקת חיסון לגוף האדם), ולייצר את החלבון האנטיגני דרך מערכת סינתזת החלבונים של התא המארח, מה שגורם למארח לייצר חסינות לתגובת החלבון האנטיגני על מנת להשיג את מטרת המניעה והטיפול במחלה.ההבדל בין השניים הוא ש-DNA מתומלל תחילה ל-mRNA ולאחר מכן מסונתז חלבון, בעוד ש-mRNA מסונתז ישירות.
03
היסטוריית הגילוי וערך היישום של חיסון mRNA
כשמדובר בחיסוני mRNA, עלינו להזכיר מדענית מצטיינת, קטי קריקו, שהניחה בסיס מחקר מדעי מוצק להופעת חיסוני mRNA.היא הייתה מלאת עניין מחקרי ב-mRNA בזמן שלמדה.במהלך יותר מ-40 שנות קריירת המחקר המדעי שלה, היא סבלה מכשלונות חוזרים ונשנים, לא פנתה לקרנות מחקר מדעי, ולא הייתה לה עמדת מחקר מדעית יציבה, אבל היא תמיד התעקשה על מחקר mRNA.
ישנם שלושה צמתים חשובים בהופעת חיסוני mRNA.
בשלב הראשון היא הצליחה לייצר את מולקולת ה-mRNA הרצויה באמצעות תרבית תאים, אך היא נתקלה בבעיה בהפעלת ה-mRNA בגוף: לאחר הזרקת ה-mRNA לעכבר, הוא ייבלע על ידי מערכת החיסון של העכבר.ואז היא פגשה את ויסמן.הם השתמשו במולקולה ב-tRNA בשם pseudouridine כדי לגרום ל-mRNA להתחמק מהתגובה החיסונית.][2].
בשלב השני, בסביבות שנת 2000, חקר פרופ' פיטר קוליס LNPs ננו-טכנולוגיות של שומנים לאספקה in vivo של siRNA ליישומי השתקת גנים [3][4].ארגון ויסמן קריקו ואח'.מצא כי LNP הוא נשא מתאים של mRNA in vivo, ועשוי להפוך לכלי בעל ערך לאספקת חלבונים טיפוליים המקודדים ל-mRNA, ולאחר מכן מאומת במניעת נגיף זיקה, HIV וגידולים [5] ][6][7][8].
בשלב השלישי, בשנים 2010 ו-2013, Moderna ו-BioNTech קיבלו ברציפות רישיונות פטנטים הקשורים לסינתזת mRNA מאוניברסיטת פנסילבניה לצורך פיתוח נוסף.קטלין הפכה גם לסגנית הנשיא הבכירה של BioNTech ב-2013 כדי להמשיך ולפתח חיסוני mRNA.
כיום ניתן להשתמש בחיסוני mRNA במחלות זיהומיות, גידולים ואסטמה.במקרה של COVID-19 שמשתולל ברחבי העולם, חיסוני mRNA עשויים למלא תפקיד כחלוץ.
04
סיכוי היישום של חיסון mRNA ב-COVID-19
עם המגיפה העולמית של COVID-19, מדינות עובדות קשה כדי לפתח חיסון לבלימת המגיפה.כסוג חדש של חיסון, חיסון mRNA מילא תפקיד מוביל בהופעתה של מגיפת הכתר החדשה.כתבי עת מובילים רבים דיווחו על תפקידו של mRNA בנגיף הקורונה החדש SARS-CoV-2 (איור 3).
איור 3 דיווח על חיסוני mRNA למניעת נגיף קורונה חדש (מ-NCBI)
קודם כל, מדענים רבים דיווחו על המחקר של חיסון mRNA (SARS-CoV-2 mRNA) נגד נגיף הקורונה החדש בעכברים.לדוגמא: חיסון ל-mRNA (mRNA-LNP) עם ננו-חלקיק-שומנים מוטבע-נוקלאוזיד, זריקה במינון יחיד משרה תגובות חזקות של תאי CD4+ T ו-CD8+ T מסוג 1, תגובת פלזמה ותאי B זיכרון ארוכי חיים ותגובת נוגדנים מנטרלת חזקה ומתמשכת.זה מצביע על כך שחיסון mRNA-LNP הוא מועמד מבטיח נגד COVID-19[9][10].
שנית, כמה מדענים השוו את ההשפעות של SARS-CoV-2 mRNA וחיסונים מסורתיים.בהשוואה לחיסוני חלבון רקומביננטי: חיסוני mRNA עדיפים בהרבה על חיסוני חלבון בתגובת מרכז הנבט, הפעלת Tfh, נטרול ייצור נוגדנים, תאי זיכרון B ספציפיים ותאי פלזמה ארוכים [11] .
לאחר מכן, כאשר מועמדים לחיסון mRNA SARS-CoV-2 נכנסו לניסויים קליניים, עלו חששות לגבי משך הזמן הקצר של הגנת החיסון.מדענים פיתחו צורה מובלעת בשומנים של חיסון mRNA שעבר נוקלאוזיד שנקרא mRNA-RBD.זריקה בודדת יכולה ליצור נוגדנים מנטרלים חזקים ותגובות סלולריות, ויכולה להגן כמעט לחלוטין על עכברי מודל שנדבקו ב-2019-nCoV, עם רמות גבוהות של נוגדנים מנטרלים שנשמרו במשך 6.5 חודשים לפחות.נתונים אלו מצביעים על כך שמנה בודדת של mRNA-RBD מספקת הגנה ארוכת טווח מפני אתגר SARS-CoV-2 [12].
ישנם גם מדענים הפועלים לפיתוח חיסונים בטוחים ויעילים חדשים נגד COVID-19, כמו חיסון BNT162b.מקוקים מוגנים מ-SARS-CoV-2, הגנו על דרכי הנשימה התחתונות מפני RNA ויראלי, ייצרו נוגדנים חזקים מאוד, ולא הראו סימנים לשיפור המחלה.שני מועמדים נמצאים כעת בהערכה בניסויים שלב I, והערכה בניסויים שלב II/III גלובליים מתקיימת גם כן, והיישום ממש מעבר לפינה [13].
05
מצב חיסון ה-mRNA בעולם
כיום, BioNTech, Moderna ו-CureVac ידועות כשלושת המובילות בעולם בטיפול ב-mRNA.ביניהן, BioNTech ומודרנה נמצאות בחזית המחקר והפיתוח של חיסון הכתר החדש.Moderna התמקדה במחקר ופיתוח של תרופות וחיסונים הקשורים ל-mRNA.חיסון ניסוי COVID-19 שלב III mRNA-1273 הוא הפרויקט הצומח ביותר של החברה.BioNTech היא גם חברת מחקר ופיתוח של תרופות וחיסונים mRNA מובילה בעולם, עם סך של 19 תרופות/חיסונים mRNA, 7 מהן נכנסו לשלב הקליני.CureVac התמקדה במחקר ופיתוח של תרופות/חיסוני mRNA, והיא החברה הראשונה בעולם שהקימה קו ייצור RNA תואם GMP, תוך התמקדות בגידולים, מחלות זיהומיות ומחלות נדירות.
מוצרים קשורים:מעכב RNase
מילות מפתח: חיסון מירנה, בידוד RNA, מיצוי RNA, מעכב RNase
הפניות: 1.K Karikó, Buckstein M, Ni H, et al.דיכוי זיהוי RNA על ידי קולטנים דמויי אגרה: השפעת שינוי הנוקלאוזיד והמקור האבולוציוני של RNA[J].חסינות, 2005, 23(2):165-175.
2. K Karikó, Muramatsu H, Welsh FA, et al.שילוב של Pseudouridine ב-mRNA מניב וקטור לא-אימונוגני מעולה עם יכולת תרגום ויציבות ביולוגית מוגברת[J].טיפול מולקולרי, 2008.3.Chonn A, קוליס יחסי ציבור.ההתקדמות האחרונה בטכנולוגיות ליפוזומים ויישומיהן לאספקת גנים מערכתית[J].Advanced Drug Delivery Reviews, 1998, 30(1-3):73.4.Kulkarni JA, Witzigmann D, Chen S, et al.טכנולוגיית ננו-חלקיקים ליפידים לתרגום קליני של siRNA Therapeutics[J].חשבונות של מחקר כימי, 2019, 52(9).5.קאריקו, קטלין, מאדן ועוד.קינטיקה של ביטוי של mRNA שעבר שינוי נוקלאוזיד הנמסר בננו-חלקיקי שומנים לעכברים בדרכים שונות [J].Journal of Controlled Release Journal of the Controlled Release Society, 2015.6.הגנה על וירוס זיקה על ידי חיסון נגד mRNA במינון נמוך בודד של נוקלאוזיד[J].טבע, 2017, 543(7644):248-251.7.Pardi N, Secreto AJ, Shan X, et al.מתן mRNA שעבר שינוי נוקלאוזיד המקודד נוגדנים מנטרלים באופן נרחב מגן על עכברים מואנשים מפני אתגר HIV-1[J].תקשורת טבע, 2017, 8:14630.8.Stadler CR, B?Hr-Mahmud H, Celik L, et al.חיסול גידולים גדולים בעכברים על ידי נוגדנים דו-ספציפיים מקודדים ל-mRNA[J].רפואת הטבע, 2017.9.NN Zhang, Li XF, Deng YQ, et al.חיסון mRNA יציב תרמי נגד COVID-19[J].תא, 2020.10.D Laczkó, Hogan MJ, Toulmin SA, et al.חיסון יחיד עם חיסוני mRNA שעברו שינוי נוקלאוזיד מעורר תגובות חיסוניות תאיות והומורליות חזקות נגד SARS-CoV-2 בעכברים - ScienceDirect[J].2020/11Lederer K, Castao D, Atria DG, et al.חיסוני mRNA SARS-CoV-2 מטפחים תגובות עוצמתיות של מרכז נבט ספציפי לאנטיגן הקשורות ליצירת נוגדנים מנטרלים[J].חסינות, 2020, 53(6):1281-1295.e5.12.Huang Q, Ji K, Tian S, et al.חיסון mRNA במינון יחיד מספק הגנה ארוכת טווח לעכברים מהונדסים מסוג hACE2 מ-SARS-CoV-2[J].תקשורת טבע.13.Vogel AB, Kanevsky I, Ye C, et al.חיסוני BNT162b אימונוגניים מגנים על מקוק רזוס מפני SARS-CoV-2[J].טבע, 2021:1-10.
זמן פרסום: 20-20-2022